Главная>
Мониторинг среды>
Загрязняющие вещества>
Загрязняющие вещества 3 класса опасности
Пыль. Взвешенные вещества.

Пыль – это вид аэрозоля, дисперсная система, состоящая из мелких твердых частиц, находящихся во взвешенном состоянии в газовой среде. Отдельные частицы или их скопления, от ультрамикроскопических до видимых невооруженным глазом, могут иметь любую форму и состав. В большинстве случаев пыль образуется в результате диспергирования твердых тел и включает частицы разных размеров, преимущественно в пределах 10-7-10-4 м. Они могут нести электрически заряд или быть электронейтральными. Концентрацию пыли (запыленность) выражают числом частиц или их общей массой в единице объема газа (воздуха). Пыль неустойчива: ее частицы соединяются в процессе броуновского движения или при оседании (седиментации).
Виды промышленной пыли:
1. Механическая пыль.
Промышленная пыль, образующаяся в результате измельчения продукта в ходе технологического процесса.
2. Возгоны.
Промышленная пыль, образующаяся в результате объемной конденсации паров веществ при охлаждении газа, пропускаемого через технологический аппарат, установку или агрегат.
3. Летучая зола.
Промышленная пыль в виде несгораемого остатка топлива, образующегося из его минеральных примесей при горении, содержащегося в дымовом газе во взвешенном состоянии.
4. Промышленная сажа.
Дисперсный углеродный продукт неполного сгорания или термического разложения углеводородов, состоящий из сферических частиц черного цвета. Средний размер сажевых частиц – 100-3500. Частицы сажи образованы из слоев углеродных атомов, подобных слоям в графите. Эти слои состоят из шестиугольников, в вершинах которых находятся атомы углерода, но, в отличии от графита, слои в саже не плоские, а изогнутые, что обуславливает сферическую поверхность частиц. Плотность сажевых частиц около 2 г/см3. Поверхность частиц в саже может быть шероховатой или гладкой.
Пыль и сажа относятся к 3 классу опасности.
ПДК вещества, мг/м3.
Максимальная разовая – 0,150
Среднесуточная – 0,05
Источники поступления пыли в атмосферу.
В воздухе содержатся частицы пыли и сажи, возникающей в результате выветривания горных пород, вулканических извержений, пожаров, ветровой эрозии пахотных земель, производственной деятельности человека. Пыль, как и другие виды аэрозолей, усиливает рассеяние и поглощение света атмосферой, влияет на ее тепловой режим.
Постоянные источники повышенной запыленности – отрасли металлургического, химического и текстильного производства, строительство и некоторые отрасли народного хозяйства (полеводство), многие транспортные средства.
Источниками выбросов сажи в атмосферу являются дизели, авиационные турбины, тепловые энергетические установки, лесные пожары и др. Концентрация сажевых частиц над океанами составляет 0,5 мкг/м3, а в приземном слое промышленно развитых районов она достигает 30 мкг/м3.
Сажа образуется при горении в промышленных и бытовых печах, при работе двигателей внутреннего сгорания (дизелях), выбрасывается вместе с продуктами горения в атмосферу в виде вредных дымов.
Сажевые частицы не взаимодействуют с кислородом воздуха, поэтому удаляются только за счет коагуляции и осаждения, которые идут достаточно медленно.
Основными источниками искусственных аэрозольных загрязнений воздуха являются ТЭС, которые потребляют уголь высокой зольности, обогатительные фабрики, металлургические, цементные, магнезитовые и сажевые заводы. Аэрозольные частицы от этих источников отличаются большим разнообразием химического состава. Чаще всего в их составе обнаруживаются соединения кремния, кальция и углерода, реже - оксиды металлов: железа, магния, марганца, цинка, меди, никеля, свинца, сурьмы, висмута, селена, мышьяка, бериллия, кадмия, хрома, кобальта, молибдена, а также асбест. Они содержатся в выбросах предприятий теплоэнергетики, черной и цветной металлургии, стройматериалов, а также автомобильного транспорта. Пыль, осаждающаяся в индустриальных районах, содержит до 20% оксида железа, 15% силикатов и 5% сажи, а также примеси различных металлов (свинец, ванадий, молибден, мышьяк, сурьма и т.д.).
Еще большее разнообразие свойственно органической пыли, включающей алифатические и ароматические углеводороды, соли кислот. Она образуется при сжигании остаточных нефтепродуктов, в процессе пиролиза на нефтеперерабатывающих, нефтехимических и других подобных предприятиях. Постоянными источниками аэрозольного загрязнения являются промышленные отвалы-искусственные насыпи из переотложенного материала, преимущественно вскрышных пород, образуемых при добыче полезных ископаемых или же из отходов предприятий перерабатываюшей промышленности, ТЭС.
Источником пыли и ядовитых газов служат массовые взрывные работы. Так, в результате одного среднего по массе взрыва (250-300 тонн взрывчатых веществ) в атмосферу выбрасывается около 2 тысяч м3 условного оксида углерода и более 150 тонн пыли.
Производство цемента и других строительных материалов также является источником загрязнения атмосферы пылью. Основные технологические процессы этих производств - измельчение и химическая обработка шихт, полуфабрикатов и получаемых продуктов в потоках горячих газов всегда сопровождается выбросами пыли и других вредных веществ в атмосферу.
Концентрация аэрозолей меняется в весьма широких пределах: от 10 мг/м3 в чистой атмосфере до 2.10 мг/м3 в индустриальных районах. Концентрация аэрозолей в индустриальных районах и крупных городах с интенсивным автомобильным движением в сотни раз выше, чем в сельской местности. Среди аэрозолей антропогенного происхождения особую опасность для биосферы представляет свинец, концентрация которого изменяется от 0,000001 мг/м3 для незаселенных районов до 0,0001 мг/м3 для селитебных территорий. В городах концентрация свинца значительно выше – от 0,001 до 0,03 мг/м3.
Влияние на живые организмы.
Пылевые частицы поглощают коротковолновую часть солнечного спектра, снижают количество достигающего земной поверхности ультрафиолета, что способствует ослаблению адаптивных свойств всех живых организмов. Они оседают на поверхности листьев растений, сокращая их способность к восприятию солнечного света.
Сажевые частицы в силу своей разветвленной поверхности способны адсорбировать значительные количества различных соединений, включая полиароматические. Таким образом, сажа играет важную роль в переносе вредных соединений в атмосфере.
Длительный контакт с сажей вызывает рак кожи, обостряются респираторные заболевания, истончается слизистая верхних дыхательных путей.
По данным Всемирной организации здравоохранения при концентрации пыли в атмосферном воздухе 0,08 мг/м3, ощущается дискомфорт у людей. При дальнейшем увеличении содержания пыли до 0,25-0,5 мг/м3 наблюдается ухудшение состояния больных с легочными заболеваниями. Постоянное пребывание людей в атмосфере с концентрацией пыли выше 0,5 мг/м3 приводит к более частым заболеваниям и возрастанию смертности.
Диоксид серы.
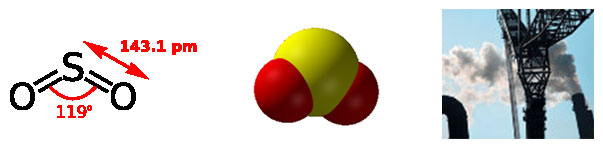
В нормальных условиях диоксид серы – бесцветный газ с характерным резким запахом (запах загорающейся спички). Растворимость газа в воде – достаточно велика.
Диоксид серы – реакционно-способен, из-за химических превращений время его жизни в атмосфере – невелико (порядка нескольких часов). В связи с этим возможности загрязнения и опасность воздействия непосредственно диоксида серы носят локальный, а в отдельных случаях – региональный характер.
Природные и антропогенные источники поступления в окружающую среду.
К природным (естественным) источникам диоксида серы относят вулканы, лесные пожары, морская пена и микробиологические превращения серосодержащих соединений. Выделяющийся в атмосферу диоксид серы может связываться известью, в результате чего в воздухе поддерживается его постоянная концентрация около 1 млн-1.
Диоксид серы антропогенного происхождения образуется при сгорании угля и нефти, в металлургических производствах, при переработке содержащих серу руд (сульфиды), при различных химических технологических процессах. Большая часть антропогенных выбросов диоксида серы (около 87%) связана с энергетикой и металлургической промышленностью. Общее количество антропогенного диоксида серы, выбрасываемое за год превышает его естественное образование в 20-30 раз.
Ежегодное поступление сернистого газа в атмосферу только вследствие промышленных выбросов оценивается почти в 150 млн. т.
Поведение в атмосфере.
Время пребывания диоксида серы в атмосфере в среднем исчисляется двумя неделями. Этого времени мало для того, чтобы газ мог распространиться в глобальном масштабе. Поэтому, в соседних географических районах, где осуществляются как большие, так и умеренные выбросы диоксида серы, в атмосфере может наблюдаться большое различие концентраций диоксида серы.
Легкорастворимый в воде, образующий кислоту газ, может разноситься мощными потоками воздуха на сотни километров (до 1500 км). При этом в облаках идет реакция образования кислот и возможно выпадение кислотных дождей.
Во время переноса диоксида серы и другие кислотные выбросы лишь в очень малой степени теряют свою активность. Нейтрализация происходит только в том случае, если в воздухе одновременно с диоксидом серы находится пыль, содержащая гидроксиды щелочных и щелочноземельных элементов. Атмосфера очищается, главным образом, при вымывании кислых газов водой и снегом, а также при их «сухом» осаждении, т.е. в виде самого газа или адсорбированного на мельчайших частицах пыли. Кроме того, диоксид серы растворяется в мельчайших капельках тумана, которые после осаждения также относят к сухой части загрязнений.
Сухая часть загрязнений обычно выпадает либо в непосредственной близости от источника выбросов, либо на незначительном удалении от него. При длительном переносе воздухом в основном выпадает связанная водой часть выбросов.
В атмосфере диоксид серы претерпевает ряд химических превращений, важнейшие из них – окисление и образование кислоты.
Окисление может проходить разными путями и в силу разных причин. Например, УФ-излучение может перевести молекулу диоксида серы в возбужденное состояние, при длине волны менее 320 нм – в синглетное возбужденное состояние, при длине волны 320-390 нм в триплетное. Молекулы диоксида серы, находящиеся в триплетном состоянии, реагируют с кислородом воздуха и через радикалы SO42- превращаются в молекулы SO3.
Большее значение все же имеет окисление с помощью радикалов ОН-. При этом возможна и реакция с озоном:
SO2 + О3 = SO3 + О2
Во влажной атмосфере образуется серная кислота.
В насыщенной парами воды фазе, например, в облаках, диоксид серы сначала образует сернистую кислоту, которая с озоном и пероксидом водорода дает серную кислоту:
Н2SО3- + О3 → SО42- + Н+ + О2
НSО3- + Н2О2 → SО42- + Н+ + Н2О
Реакционный пероксид водорода может образоваться из органических пероксидов во влажном воздухе.
Как диоксид серы, так и НSО3- в несколько промежуточных стадий могут превратиться в серную кислоту с помощью ионов металлов, которые могут присутствовать в воздухе, а также в облаках.
Сернистый газ с водой воздуха образует капельки серной кислоты. Растворы серной кислоты могут долго держаться в воздухе в виде плавающих капелек тумана или выпадать вместе с дождем на землю. Эти растворы разъедают металлы, краски, синтетические соединения, ткани, губительно действуют на растения и животных. Попадая на землю, серная кислота подкисляет почвы. В результате этого сокращается почвенная фауна, что отрицательно сказывается на урожае.
Воздействие на живые организмы.
Класс опасности вещества – 3.
При повышенной концентрации пыли токсическое действие диоксида серы проявляется значительно сильнее, чем в воздухе, свободном от пыли.
Комбинация диоксида серы с оксидами азота значительно увеличивает число заболеваний дыхательных путей.
При среднесуточной концентрации сернистого газа 0,1-0,2 мг/м3 у населения наблюдается обострение заболеваний верхних дыхательных путей. Резкое увеличение числа случаев заболеваемости бронхитами у людей старше 55 лет отмечается на следующий день после повышения среднесуточной концентрации сернистого газа до 0,7 мг/м3.
Повышение уровня загрязнения сернистым газом вызывает либо хроническое, либо острое кратковременное поражение листьев растений, что приводит к замедлению роста зеленой массы и снижению урожайности. Разрушается хлорофилл растений, повреждаются листья и хвоя. Пораженные участки приобретают бронзовую окраску. На листьях также появляются бледные пятна, которые затем приобретают бронзовый цвет, затем листья опадают. Наиболее чувствительными к диоксиду серы являются хвойные деревья. Сосна погибает при среднегодовой концентрации сернистого газа 0,18-0,20 мг/м3. Лиственные деревья начинают поражаться при концентрации диоксида серы от 0,5 до 1 мг/м3.
Оксиды серы ощутимо ускоряют в городах коррозию металлов - в 1,5-5 раз по сравнению с сельской местностью. В одном из городов США увеличение концентрации SO2 в 3 раза сопровождалось увеличением скорости коррозии цинка в 4 раза.
Особенно опасно для растений высокое содержание сернистого газа, например, при интенсивном освещении и большой относительной влажности воздуха, а также на стадиях цветения и плодоношения. Хроническое повреждение листьев растений происходит в результате постепенного накопления в их тканях избыточного количества сульфатов. Сульфаты также окисляют почву и снижают ее плодородие.
Магний.
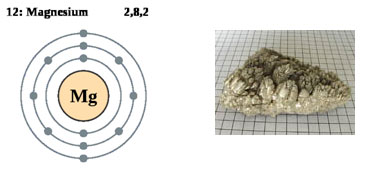
Магний – элемент II группы, в земной коре содержится порядка 1,87 массовой доли магния. Магний – характерный элемент мантии Земли. В магматических процессах магний – аналог железа.
Миграция в окружающей среде
В биосфере наблюдается энергичная миграция и дифференциация магния: здесь главная роль принадлежит физико-химическим процессам - растворению, осаждению солей, сорбции магния глинами. Магний слабо задерживается в круговороте веществ на континентах и с речным стоком поступает в океаны. Морская вода не насыщена магнием и осаждение его солей не происходит. При испарении морской воды магний снова попадает на континенты.
Влияние на живые организмы
Магний – постоянная и необходимая часть растительных и животных организмов, входит в состав всех органелл клеток. Магний входит в состав хлорофилла растений, активирует многие ферменты живых организмов.
В человеческом организме накапливается в печени, затем переходит в кости и мышцы. Магний – антагонист кальция в организме, при избытке магния, при рахите он может вытеснять кальций из костей.
Соединения магния относятся к 3 классу опасности по воздействию на людей.
«назад» |